Din cuprinsul articolului
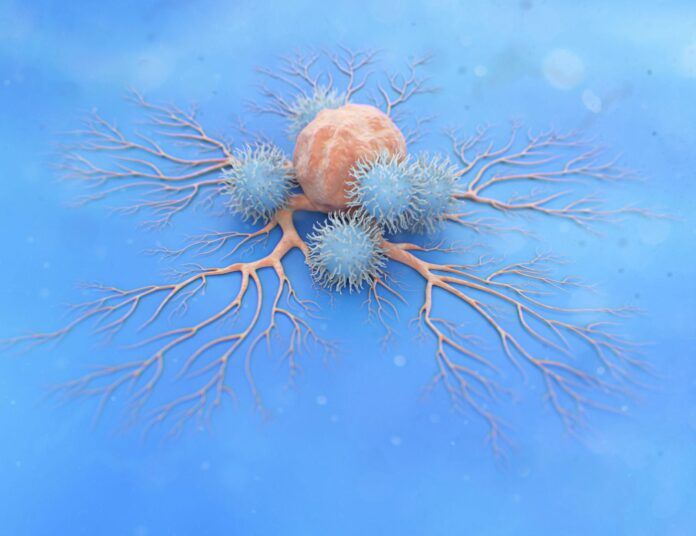
O echipă de la Centrul de Terapie Celulară din Ribeirão Preto, afiliat University of São Paulo, a demonstrat că modificarea fină a „circuitelor interne” ale celulelor Natural Killer poate crește semnificativ capacitatea acestora de a distruge celulele tumorale.
Rezultatele, publicate în noiembrie 2025 în Frontiers in Immunology, descriu o nouă generație de celule CAR-NK cu activare mai rapidă, citotoxicitate crescută și posibilitate de control farmacologic temporar.
Studiul oferă date preclinice care ar putea influența dezvoltarea viitoarelor terapii celulare pentru cancere hematologice și, potențial, pentru tumori solide.
Ce au făcut cercetătorii
Echipa a folosit linia celulară NK-92, un model standard în cercetarea imunoterapiei, și a testat noi variante de receptori chimerici antigenici, cunoscuți drept CAR. Aceste structuri permit celulelor imune să recunoască ținte specifice de pe suprafața celulelor canceroase.
În interiorul receptorului, cercetătorii au introdus domenii costimulatoare 2B4 și DAP12. Aceste componente funcționează ca amplificatoare de semnal, influențând intensitatea răspunsului imun după ce celula NK identifică tumora.
Rezultatul: celulele modificate au prezentat o stare de activare mai pronunțată și o capacitate crescută de distrugere a celulelor tumorale comparativ cu versiunile standard.
De ce este diferit față de terapia CAR-T
Terapia CAR-T a schimbat prognosticul unor cancere hematologice, însă majoritatea cunoștințelor privind designul receptorilor provin din studii pe limfocite T. Celulele NK au mecanisme distincte de activare și reglare.
Transferarea directă a „rețetelor” din CAR-T către CAR-NK nu oferă întotdeauna aceleași rezultate. Tocmai de aceea ajustarea domeniilor costimulatoare reprezintă un pas esențial pentru eficiență și siguranță.
Autorii arată că optimizarea semnalelor interne poate transforma celulele NK într-o platformă terapeutică mai stabilă și mai predictibilă.
Control farmacologic temporar cu dasatinib
Un element suplimentar al studiului a fost utilizarea dasatinibului, un inhibitor de tirozin kinază deja utilizat în oncologie.
În acest context, medicamentul a fost administrat temporar pentru a modula activarea celulelor CAR-NK. Modelele animale au indicat că combinația dintre designul 2B4-DAP12 și pretratamentul cu dasatinib a dus la un control tumoral superior comparativ cu variantele tradiționale.
Această abordare oferă un avantaj important: posibilitatea reglării activității celulelor fără modificări genetice permanente suplimentare. Controlabilitatea este una dintre preocupările majore în terapia celulară, unde un răspuns imun excesiv poate genera reacții adverse severe.
Contextul mai larg al terapiei cu celule NK
Celulele NK fac parte din imunitatea înnăscută și au capacitatea naturală de a identifica și elimina celule infectate sau transformate malign, fără necesitatea unei sensibilizări prealabile.
În ultimii ani, interesul pentru CAR-NK a crescut datorită unor avantaje potențiale:
-
risc mai redus de sindrom de eliberare de citokine comparativ cu CAR-T
-
posibilitatea utilizării unor produse „off-the-shelf”
-
profil imunologic diferit
Finanțarea cercetării a fost asigurată de São Paulo Research Foundation, prin programul RIDC.
Ce urmează
Rezultatele sunt preclinice și necesită validare în studii clinice pe pacienți. Nu există încă date privind eficiența sau siguranța la om pentru această configurație specifică de CAR-NK.
Totuși, studiul indică o direcție clară: terapia celulară poate fi ajustată la nivel molecular pentru a deveni mai precisă și mai eficientă. În oncologie, unde rezistența la tratament rămâne o problemă majoră, astfel de optimizări pot face diferența între un răspuns parțial și unul durabil.
Pe termen scurt, cercetarea adaugă o piesă nouă în puzzle-ul imunoterapiei. Pe termen lung, ar putea contribui la dezvoltarea unor terapii celulare mai accesibile, mai controlabile și mai eficiente împotriva cancerului.