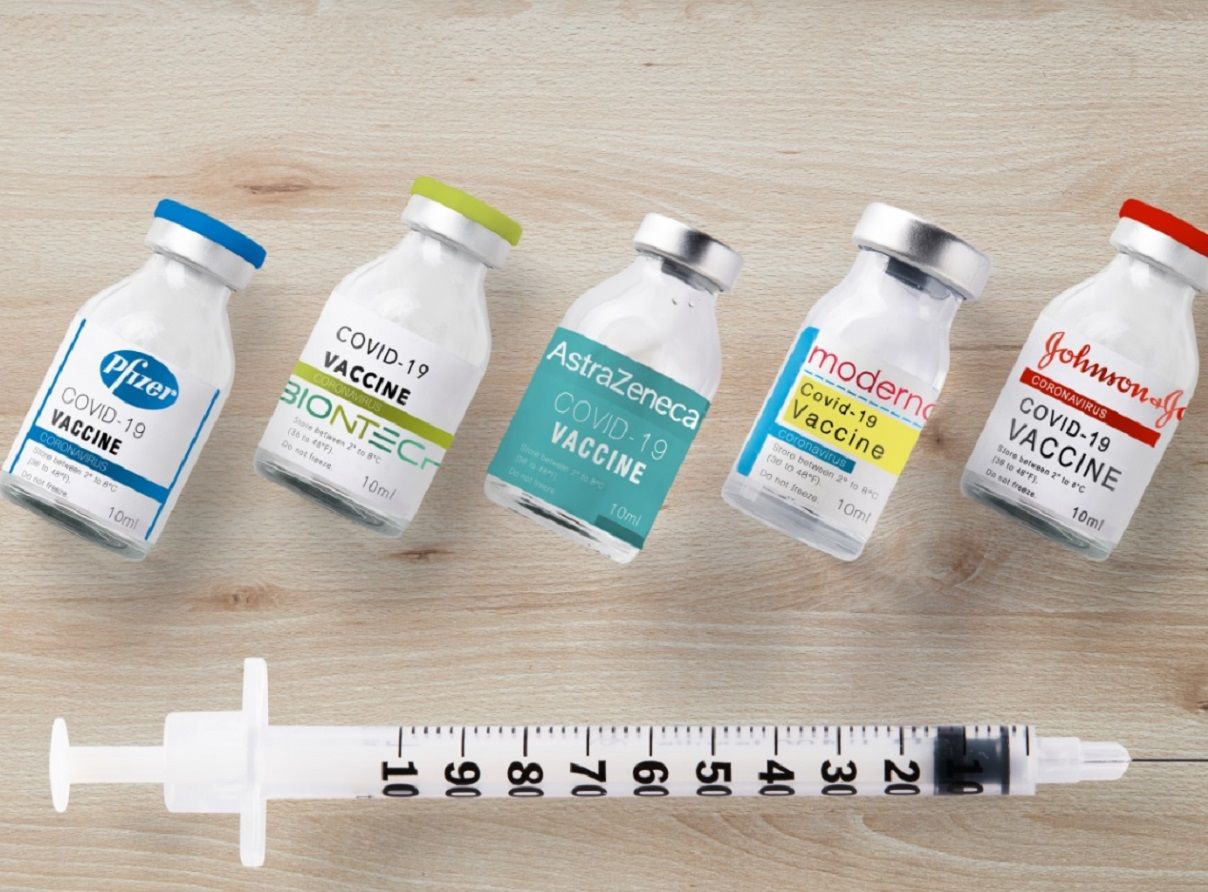
Vaccinările Johnson & Johnson au fost întrerupte după apariția unor cazuri rare de coagulare
Oficialii federali din domeniul sănătății au cerut oprirea utilizării vaccinului coronavirus al companiei în timp ce studiază bolile grave care s-au dezvoltat la șase femei americane, conform New York Times.
Injecțiile cu vaccinul coronavirus Johnson & Johnson s-au oprit brusc în Statele Unite, după ce agențiile federale de sănătate au cerut o pauză în utilizarea vaccinului, deoarece examinează o tulburare rară de coagulare a sângelui care a apărut la șase destinatari.
Toate cele șase erau femei cu vârste cuprinse între 18 și 48 de ani și toate au dezvoltat boala în decurs de una până la trei săptămâni de la vaccinare. O femeie din Virginia a murit, iar o a doua femeie din Nebraska a fost internată în stare critică.
Peste șapte milioane de oameni din Statele Unite au primit până acum vaccinul Johnson & Johnson și alte 10 milioane de doze au fost expediate către state, potrivit datelor Centrelor pentru Controlul și Prevenirea Bolilor.
„Recomandăm o pauză în utilizarea acestui vaccin dintr-o abundență de precauție”, a spus dr. Peter Marks, directorul Centrului de evaluare și cercetare a produselor biologice al Food and Drug Administration și dr. Anne Schuchat, directorul adjunct principal al CDC, într-o declarație comună. „În acest moment, aceste evenimente adverse par a fi extrem de rare.”
În timp ce au încadrat această mișcare ca o recomandare pentru medicii, impactul a fost imediat. Marți seară, fiecare stat, districtul Columbia și Puerto Rico au anunțat o pauză în vaccinarea cu vaccinul Johnson & Johnson.
Dincolo de țărmurile americane, Johnson & Johnson a declarat că va întârzia lansarea vaccinului său în Europa, unde mai multe țări sunt pregătite să înceapă să îl administreze săptămâna aceasta. Africa de Sud, devastată de o variantă mai contagioasă a virusului care a apărut acolo, a suspendat și ea utilizarea vaccinului. Australia a anunțat că nu va cumpăra nicio doză.
Într-o declarație, Johnson & Johnson a declarat că susține „comunicarea deschisă” cu profesioniștii din domeniul sănătății și cu publicul și că a lucrat îndeaproape cu experți medicali și autoritățile din domeniul sănătății, inclusiv în Europa. „Am luat decizia de a întârzia proactiv lansarea vaccinului” acolo, a spus firma.
Compania a mai spus că întrerupe vaccinările în studiile sale clinice. În prezent, testează eficacitatea a două doze, spre deosebire de doza unică care a fost autorizată în februarie.
Numai în Statele Unite, 300.000 până la 600.000 de oameni pe an dezvoltă cheaguri de sânge, potrivit datelor furnizate de C.D.C.. Dar cele șase cazuri care au dus la pauză vaccinării au implicat o combinație rară de simptome. Cheagurile au apărut în creier, într-o afecțiune numită tromboză a sinusului venos cerebral. Cheagurile au fost însoțite de niveluri scăzute de trombocite, o componentă a sângelui care ajută la formarea cheagurilor care în mod normal ajută la vindecarea rănilor.
Toate femeile au dezvoltat boala în decurs de aproximativ una până la trei săptămâni de la vaccinare, cu un timp mediu de nouă zile.
Femeia spitalizată din Nebraska,în vârstă de 40 de ani a dezvoltat cheaguri de sânge la două săptămâni după vaccinare, au declarat oficialii de sănătate de stat.
Femeia din Virginia, în vârstă de 45 de ani, a dezvoltat simptome la șase zile după ce a fost inoculată la începutul lunii martie și a murit la șase zile după aceea, au spus oficialii din domeniul sănătății. Ei au spus că atenția publică generează deja o serie de noi rapoarte de posibile cazuri către autoritățile federale.
Preocupările cu privire la vaccinul Johnson & Johnson le reflectă pe cele despre AstraZeneca. Autoritățile de reglementare europene au început să investigheze acest vaccin luna trecută, după ce unii beneficiari au dezvoltat cheaguri de sânge și un număr scăzut de trombocite, precum cele ale beneficiarilor Johnson & Johnson.
Din 34 de milioane de persoane care au primit vaccinul AstraZeneca în Marea Britanie, Uniunea Europeană și alte trei țări, 222 au experimentat cheaguri de sânge legate de un nivel scăzut de trombocite. Majoritatea acestor cazuri au implicat femei sub 60 de ani.
Pe 7 aprilie, Agenția Europeană pentru Medicamente, principala agenție de reglementare, a concluzionat că tulburarea a fost un efect secundar foarte rar. Autoritățile de reglementare europene au susținut că beneficiul vaccinului AstraZeneca a depășit cu mult acest mic risc. Țările din Europa și din alte părți au continuat să administreze vaccinul persoanelor în vârstă, care sunt mai expuse riscului de coronavirus.
Atât Johnson & Johnson, cât și AstraZeneca folosesc adenovirusuri pentru a transporta ADN-ul în celulele umane pentru a începe procesul de generare a imunității la coronavirus. Nu se știe încă dacă această tehnologie comună determină coagularea în cazuri rare.